El "bardo" entre Bohr y Einstein (Parte I)
Ciencia y Educacion 03.05.2014 a las 18:15 hs 1492 2


Cita:El debate Bohr Einstein es un nombre popular dado a una serie de disputas públicas entre Albert Einstein y Niels Bohr acerca de la física cuántica. Sus "debates" son muy recordados debido a su importancia en la filosofía de la ciencia. El sentido y significación de estos debates son escasamente comprendidos, pero su gran importancia fue tenida en cuenta por el propio Bohr y escrita en su artículo "Discusiones con Einstein sobre los Problemas Epistemológicos en la Física Atómica" publicados en un volumen dedicado a Einstein.
concienzuda no me han llevado
más cerca de la respuesta a la
pregunta, ¿qué son los cuantos de luz?
Hoy día todo Juan, Pepe o Pancho
cree que sabe, pero está equivocado.
Sigo creyendo en la posibilidad de
construir un modelo de la realidad,
es decir, de una teoría que represente
las cosas en sí mismas y no sólo la
probabilidad de su ocurrencia.
A. EINSTEIN

LA MECÁNICA CUÁNTICA
Se considera que en 1925-1926 quedó constituida la mecánica cuántica en la forma en que hoy la conocemos. Ahora veremos una nueva faceta de Einstein estrechamente vinculada con las teorías cuánticas. Para facilitar la lectura se dividirá este post en 2 partes, en esta primera parte se verá cómo se llegó a esta teoría y en qué consiste.

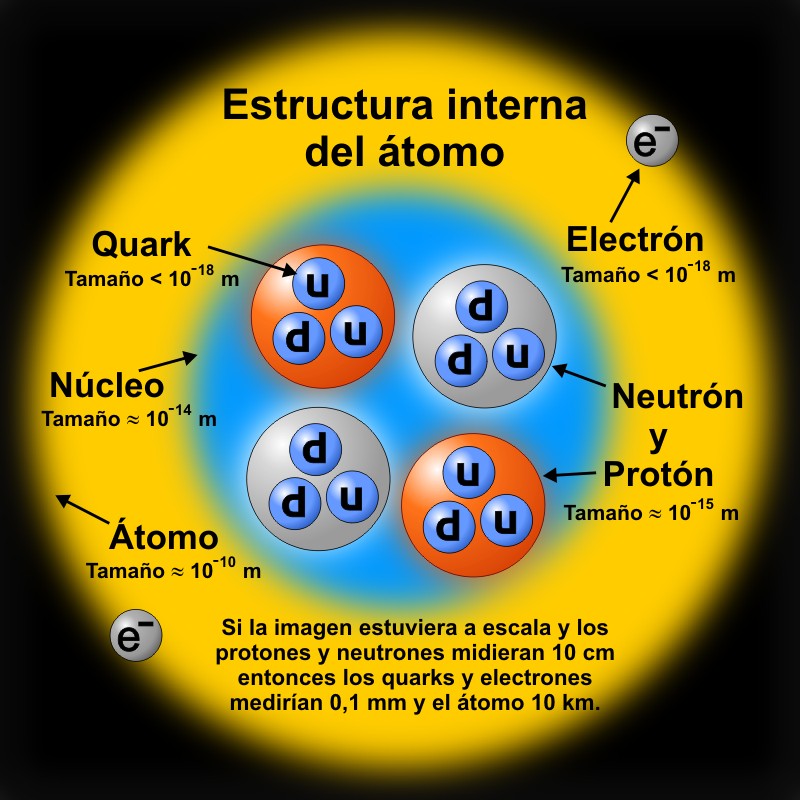
Hacia 1911 el extraordinario físico experimental británico de origen neozelandés Ernest Rutherford (1871-1937) había llegado a la conclusión de que los átomos tienen una estructura similar a la de un sistema planetario en miniatura —ésta es la imagen usual que vemos en los textos elementales y las películas de ciencia ficción—: que están formados por un núcleo pequeñísimo y los electrones se encuentran orbitando alrededor de él. Como el átomo es eléctricamente neutro, el núcleo tiene una carga positiva tal que neutraliza la carga negativa de los electrones; esta carga se debe a los protones que contiene. Como los electrones son sumamente ligeros (1 840 electrones tienen una masa aproximadamente igual a la de un solo protón), prácticamente toda la masa del átomo está concentrada en el núcleo. Pero explicar las propiedades de estos átomos fue una tarea que demandó el esfuerzo continuado de muchos investigadores —incluidos prácticamente todos los grandes físicos del periodo— durante muchos años.
Es complicada la historia de la teoría cuántica, es decir, de la teoría de los átomos y sistemas compuestos por ellos. Para resumir se puede decir que se inicia con un modelo muy simple, pero audaz, propuesto por el físico danés Niels Bohr (1885-1962) en 1913, capaz de predecir muchas propiedades del átomo de hidrógeno, aunque inadecuado para ir más lejos. A partir de los trabajos de Bohr se inicia una búsqueda que culmina en una teoría propuesta por el joven físico alemán Werner Heisenberg (1901-1976) en 1925 y desarrollada de inmediato por Max Born y su joven asistente, el matemático Pascual Jordan (1902-1984). Paralelamente se desarrolla otra dirección independiente de investigación, surgida de una proposición del físico francés Louis de Broglie (1892- ), en la que Einstein tiene una intervención decisiva y la que es llevada a sus últimas consecuencias por Erwin Schrödinger (físico austriaco, 1887-1961). Este esfuerzo culminó en 1926 con una versión diferente, pero equivalente a la anterior, de la mecánica cuántica. Finalmente, el joven físico inglés Paul Dirac (1902-1984) reformuló matemáticamente en 1926 las teorías disponibles y les dio la forma de la actual mecánica cuántica, aunque fue Niels Bohr quien contribuyó más decididamente a darle su contenido interpretativo actual.
Vamos a repasar ahora algunas de las propiedades más importantes y características de los sistemas cuánticos —como podrían ser átomos, moléculas, cristales, o incluso estructuras más complejas constituidas por estos elementos, pero normalmente de tamaño microscópico

LAS PROPIEDADES DISCRETAS
La que tal vez constituye la característica más general de los sistemas cuánticos, es que algunas de sus propiedades pueden tomar sólo valores discretos, discontinuos. Ésta fue la propiedad que descubrió Planck en lo que se refiere a la energía intercambiada entre el campo electromagnético y las paredes de la cavidad y que fue reinterpretada por Einstein como producto de que las partículas que componen al campo poseen precisamente la energía hf cada una. Como vimos, Planck usó esta propiedad para introducir el término quanto, de donde se deriva el nombre de la teoría. Como un análogo que puede servir para aclarar las ideas, es posible pensar en los sonidos producidos por un piano: podemos producir una nota, o la siguiente, o la siguiente, y así sucesivamente, pero no podemos producir ningún sonido entre dos notas: decimos que los sonidos del piano tienen un espectro discreto, discontinuo; es la forma convencional de referirnos a esta propiedad.

El hecho de que la energía de los electrones de un átomo sea discreta es muy importante; esto significa, por ejemplo, que el tamaño de todos los átomos de hidrógeno en su estado normal, es el mismo: no hay átomos de H chicos y grandes: todos son iguales y tienen el mismo tamaño y las mismas propiedades. Sin embargo, si calentamos el H o le suministramos energía en cualquier otra forma, algunos átomos absorberán una parte de la energía en exceso, otros otra parte y así sucesivamente, y aparecerá toda una serie de valores discretos posibles de energía, como las notas del piano. Ahora, cuando se enfría este H los átomos empiezan a emitir la energía que les sobra, saltando de una energía a la otra; como la energía se conserva en éstos saltos —como en cualquier fenómeno natural— la diferencia de las energías entre las órbitas inicial y final aparece en la forma de un fotón

lo que podemos escribir como sigue:
Esta fórmula nos muestra algo sumamente importante: la radiación electromagnética emitida por los átomos al enfriarse, tiene frecuencias, es decir, colores, perfectamente definidos, que forman un espectro discreto. De hecho, estamos narrando la historia al revés: lo primero que se descubrió es que cada elemento posee un espectro de emisión discreto que le es característico —algo así como su huella digital electromagnética— y sólo muchas décadas después Bohr pudo explicar este hecho con la fórmula anterior, que resultaba de su teoría.

Cita:Ahora bien, la mecánica cuántica no describe en detalle cómo se realizan estos saltos. Como, por otra parte y según veremos más adelante, la noción de trayectoria tampoco es propia de esta teoría, con frecuencia se supone que los saltos cuánticos se realizan en forma instantánea, sin que "exista" ni "pase" nada intermedio. No se asuste el lector: todavía tendrá ocasión para las sorpresas.
LAS PROPIEDADES ONDULATORIAS
Vimos como en su ponencia de Salzburgo en 1909 Einstein avanzó una profética observación: la descripción de los sistemas cuánticos tendría que incorporar tanto aspectos corpusculares como ondulatorios. El darle forma definida a esta hipótesis fue el gran descubrimiento de Louis de Broglie, quien en 1923 y después en su tesis doctoral de 1924 propuso la idea de que a todo movimiento es necesario asociar una onda, y dio una fórmula para hacerlo. A partir de este descubrimiento de De Broglie pronto se construyó la llamada mecánica ondulatoria, que es una de las versiones originales de la mecánica cuántica. Esto quiere decir, por ejemplo, que un electrón bajo ciertas condiciones se comporta como un corpúsculo (por ejemplo, en el efecto Compton, es decir, cuando choca con un fotón), pero que en otras circunstancias se puede comportar como una onda (por ejemplo, en el microscopio electrónico).

Einstein mismo avanzó considerablemente en esta dirección, hecho que es poco conocido. En 1925 preparó un trabajo, estimulado por las novedosas y atinadas observaciones del físico indio Satyendra Bose (1894-1974), en el cual se muestra que sistemas cuánticos, como los gases, no deben describirse usando métodos estadísticos clásicos (los de Maxwell y Boltzmann), sino con la ayuda de una nueva estadística de tipo cuántico (y que hoy se llama de Bose-Einstein). Para estudiar estos gases cuánticos, Einstein regresó a su viejo método de 1909 de las fluctuaciones y encontró que para obtener los resultados correctos, a las fluctuaciones de la energía producidas por el movimiento de las moléculas del gas tenía una vez más que agregar un término adicional, ahora idéntico al producido por la interferencia de ondas clásicas como la luz. Así, Einstein cierra elegantemente un círculo lógico abierto 20 años antes: tanto para la descripción del campo electromagnético, como para la de las moléculas, se requieren simultáneamente términos corpusculares y ondulatorios. Einstein señala que esta conclusión es más que una mera analogía y menciona que ha conocido en esos días la proposición de De Broglie —Paul Langevin (físico francés, 1872-1946) le había enviado una de las copias de la tesis—. Concluye que un campo ondulatorio debe estar conectado a cada cuerpo en movimiento en forma análoga a como el campo ondulatorio óptico está conectado con el movimiento de los cuantos de luz; seguramente, sugiere, este fenómeno ondulatorio se podría observar mediante fenómenos de difracción. 4 Anota entonces algunas características de está onda y aplica la idea al estudio de ciertas propiedades térmicas de los gases. Esta onda de Einstein es la que unos meses después toma Schrödinger como base para construir la versión ondulatoria de la mecánica cuántica.
Las propiedades ondulatorias de los electrones son extraordinariamente importantes. Por ejemplo, ellas indican que los electrones pueden comportarse como si fueran ondas bajo ciertas circunstancias, pero en otras como si fueran corpúsculos. A esto se refiere uno cuando se habla de la dualidad onda-corpúsculo. También es característico de los sistemas cuánticos que nunca se observan las propiedades ondulatorias y las corpusculares juntas:se manifiesta una o la otra. A esto se hace referencia diciendo que ambas propiedades son complementarias. La interpretación física que usualmente se da a estos hechos es la siguiente. Cuando el electrón se comporta como corpúsculo se encuentra esencialmente localizado en un punto; pero cuando el electrón se manifiesta como una onda se encuentra distribuido en todo el espacio ocupado por a onda. Que se manifieste en una u otra de estas formas depende de la situación específica, por lo que el experimentador está en condiciones de inducir la manifestación de uno u otro aspecto, si lo desea.

No se pierdan la segunda parte del tema
Una publicación gracias a nuestros patrocinadores


Puntos: 280
Comentarios (11)
Medallas
Posts Relacionados:




